【研究ツールとしての抗体技術】抗原とエピトープ
抗体技術の基本原理
免疫化学を活用した抗体技術は、1970年代初期に免疫標識の研究ツールとして用いられて以降、大きく進歩し、ライフサイエンス研究の多くの分野において必要不可欠なツールとなっています。免疫化学の基本原理は「特異的な抗体が、特定の抗原と結合し、ユニークな組み合わせの抗原抗体複合体を形成する」ということです。
この記事では、免疫化学および抗体技術を理解するために重要な要素である「抗原」と、抗原に抗体が結合する部位である「エピトープ」について、解説します。
抗原とは何か
抗原とは、免疫反応(例:特異抗体分子の産生)を誘発する能力を持つすべての物質を指します。英語のantigen(抗原)は、antibody generation(抗体産生)に由来し、Agと略記されることもあります。抗原は、その抗原の存在によって形成された特異抗体に結合する能力を持っています。
一般的に、抗原は異種タンパク質(ホストの身体を構成するものとは異なるタンパク質)またはその断片であり、感染によってホストの体内に侵入します。しかし、場合によっては、ホスト自身のタンパク質が抗原として作用し、自己免疫反応を誘発することもあります。細菌やウイルスは表面か内部に抗原を持っているため、これらの抗原を分離し、ワクチンの開発に用いることができます。
抗原となり得る物質
抗原は一般的に分子量が高く、通常はタンパク質または多糖類です。ポリペプチド、脂質、核酸、その他の様々な成分が抗原として機能することもあります。また、ハプテンと呼ばれる小さな物質が、ウシ血清アルブミン、キーホールリンペットヘモシアニン(KLH)、またはその他の合成マトリックスなど、より大きなキャリアタンパク質と化学的に結合している場合は、これらに対しても免疫反応が誘発されることがあります。
薬剤、単糖、アミノ酸、低分子ペプチド、リン脂質、またはトリグリセリドなどの多様な分子が、ハプテンとして機能する場合があります。このように、十分な時間をかければ、すべてのあらゆる異物が免疫系によって特定され、特異抗体の産生を誘発し得るということになります。しかし、この特異的な免疫反応は非常に可変的で、抗原のサイズ、構造、組成に大きく依存しています。タンパク質または糖タンパク質は、強力な免疫反応を誘発する能力がある、つまり、免疫原性が高いため、最も適した抗原とされています。
<優れた抗原の特性>
- 分子内に構造的安定性および化学的複雑性を有する領域がある
- 相当な長さがあるが、大規模な反復単位がない
- 分子量が最小でも8,000〜10,000 Daである(ただし、キャリアタンパク質の存在下では、分子量が200 Da程度のハプテンも用いられる)
- 免疫系によって処理可能である
- 抗体形成機構が到達可能な免疫原性領域がある
- ホスト内に存在するものとは十分に異なった構造エレメントがある
- ペプチド抗原の場合、K、R、E、D、Q、Nの免疫原性アミノ酸を30%以上含有する領域がある
- ペプチド抗原の場合、親水性、または帯電したアミノ酸残基がある
抗原の認識プロセス
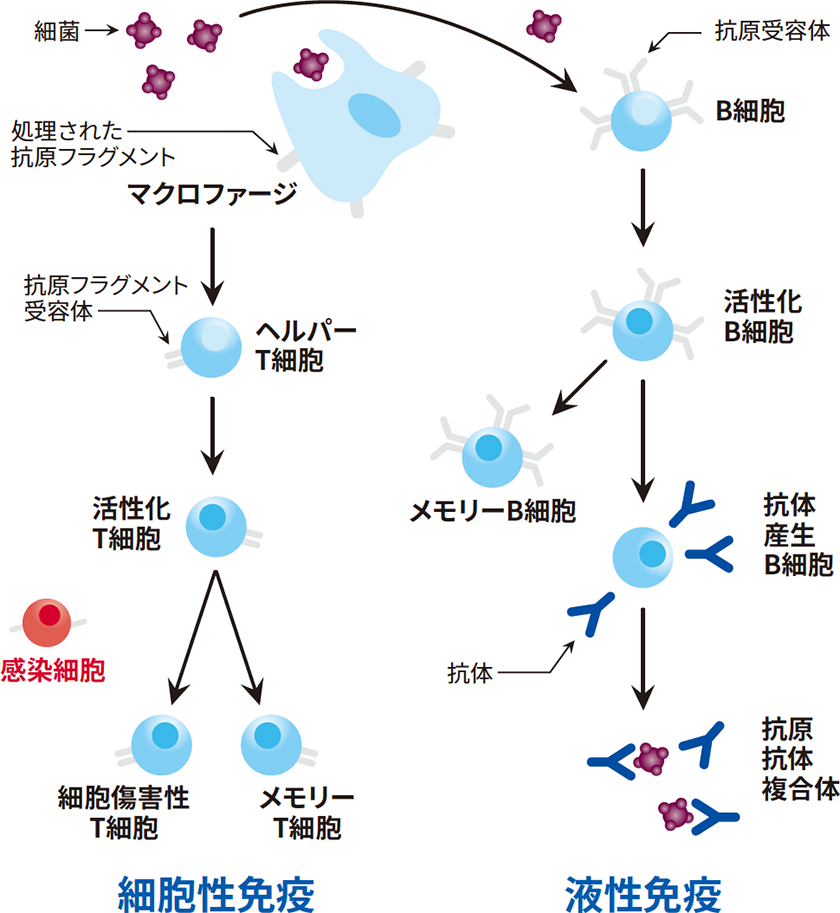
抗原は、「B細胞およびその表面抗体(sIgM)」と「T細胞上のT細胞受容体」の2種類の異なる工程によってホストに認識されます。B細胞もT細胞も同じ抗原に反応しますが、反応するのは抗原分子上の別々の部分です。B細胞の表面にある抗体は、タンパク質の立体構造を認識することができます。一方、T細胞では、抗原が抗原提示細胞によって取り込まれ、認識可能なフラグメントに分解される必要があります。一般的な抗原提示細胞は、マクロファージや樹状細胞です。下の図は、免疫反応のプロセスをまとめたものです。
免疫反応の図
エピトープとは
抗原には、相補的な抗体が特異的に結合する小さな部位があり、これをエピトープまたは抗原決定基と呼びます。エピトープは通常、抗原の表面にある1~6個の単糖または5~8個のアミノ酸残基で構成されています。
抗原分子は三次元の立体構造を持つため、抗体によって認識されるエピトープは、抗原の特定の立体構造に依存している場合があります。例えば、天然タンパク質の2つのループまたはサブユニットの相互作用によって形成されるユニークな部位が挙げられます。このようなエピトープを構造的エピトープ(不連続エピトープ)といいます。一方、単純な直鎖状アミノ酸配列によって構成される場合は線状エピトープ(連続エピトープ)といいます。
標的分子(抗原)上の潜在的な結合部位は多岐にわたり、そのそれぞれが、共有結合、イオン結合、親水性および疎水性相互作用によって、独自の構造的特性を持っています。これが抗体の選択や性能に重大な影響を及ぼします。標的抗原と抗体の間に効率的な相互作用を生じさせるためには、エピトープが容易に結合可能でなければなりません。
変化するエピトープ
標的分子が、固定、還元、pH変化、またはゲル電気泳動の前処理によって変性してしまった場合には、エピトープが変化し、抗体と相互作用する能力に影響することあります。例えば、一部の抗体はウェスタンブロット(WB)では機能しませんが、免疫組織化学(IHC)には適しています。これは、IHCの手順では、複雑な抗原部位が組織中で維持される可能性があるのに対し、WBではサンプル調製の工程によってタンパク質の立体構造が変化し、抗原部位が破壊され抗体と結合できなくなってしまうためです。
変性タンパク質では、線状エピトープ以外は認識されない場合があります。したがって、ウェスタンブロットなどの変性タンパク質を用いるプロトコールでは、線状エピトープを認識する抗体を使用しましょう。
エピトープは、折り畳まれたタンパク質の内部にある場合もあります。このようなエピトープは、免疫沈降法などの変性を伴わないプロトコールでは抗体に接近することができません。一方、立体構造エピトープは、折り畳まれたタンパク質の外側にあります。立体構造エピトープを認識する抗体は、免疫沈降法またはフローサイトメトリーなどの穏やかで変性を伴わない手順に適しています。
通常折り畳まれているタンパク質の表面にある線状エピトープを認識する抗体であれば、変性を伴うプロトコールでも伴わないプロトコールでも良好に機能します。
このようにエピトープは、抗原の自然な細胞環境において存在している場合もあれば、変性後においてのみ露出される場合もあります。自然状態では、抗原は細胞質性(可溶性)、膜結合性、または分泌性である場合があります。エピトープの数、位置、サイズは、抗体が産生される際に、どの状態の抗原が提示されているかによって変化します。
標的タンパク質、抗体によって認識されるエピトープ、配列保存性、技術的原則に関する知識は、抗体やプロトコールの選択に役立ちます。ただし、実際のエピトープマッピングまたは配列データは、有用ではありますが抗体の特異性を確定するために必要なわけではありません。
以上、抗体技術の基本原理を理解するために重要な「抗原」と「エピトープ」について解説しました。技術を適切に利用し試行錯誤するためには、原理をきちんと把握することが大切です。抗体を使用した実験を始める前には一度、抗体と抗原について復習してみましょう。
抗体がよくわかる!「抗体ガイドブック 3版」。
この記事以外にも抗体そのものの理論や選び方が分かる記事あります。
理論
- 【研究ツールとしての抗体技術】抗原とエピトープ
- 抗体の仕組みと種類を理解しよう
- 抗原と抗体の相互作用とは【抗体技術の基本原理】
- モノクローナル抗体とポリクローナル抗体の作製と特徴
- 用途に合わせて使い分け。抗体のフォーマットと精製方法
実用
これら抗体の理論や実用、応用、プロトコールの例を掲載した「抗体ガイドブック 3版」をご用意しています。こちらのページで印刷版の請求またはPDFのダウンロードが可能です。

下記フォームでは、M-hub(エムハブ)に対してのご意見、今後読んでみたい記事等のご要望を受け付けています。
メルクの各種キャンペーン、製品サポート、ご注文等に関するお問い合わせは下記リンク先にてお願いします。
*入力必須