DIGシステムにおけるRNAプローブ作成方法

DIGシステムにおけるRNAプローブ作成方法
ハイブリダイゼーションは核酸分子が相補的に結びついて二本鎖を形成すること、およびそれを活用した実験方法をさします。ハイブリダイゼーションによって核酸を検出するには、RI(放射性同位元素)を用いる方法と、抗原抗体反応と化学発光を利用する方法とがあり、DIGシステムは後者のひとつです。この方法では、ステロイドハプテンであるDigoxigenin(ジゴキシゲニン)を結合させたUTPをプローブ中に取り込ませることによって標識を行います。
DIGによる標識は、RIを使用しないため安全性が高く、短い露光時間で検出が可能であるなど様々な利点があります。DNA、RNA、オリゴヌクレオチド、いずれの核酸の標識にも使用することができますが、この記事では、特にDIGを用いてRNAを標識する方法や注意点について紹介します。
in vitro転写によるRNAの標識
アプリケーションによってはDIG標識RNAは、DIG標識DNAよりもずっと効果的なハイブリダイゼーション・プローブとなりえます。例えば、数ngオーダーのトータルRNA中からレアなmRNAを検出する場合などが挙げられます。
標識RNAプローブは、DNAテンプレートからのin vitro転写によって合成されます。まず、転写するDNAを、プロモーター(T7、SP6、またはT3 RNAポリメラーゼ)を含む、適切な転写ベクターのマルチクローニングサイト(MCS)にクローニングします。
次に、テンプレートDNAを挿入部位に近い適切なベクターの部位で開裂し、直鎖化します。RNAポリメラーゼはDIG-UTPを含むリボヌクレオチド混合物の存在下で、DNAインサートをアンチセンスRNAへと転写。数百回におよぶDNA転写を経て、完全長のDIG標識RNAプローブが得られます。これによって、通常1µgのDNAから10~20µgのRNAを取得できます。
この手法では、RNAの約25~30塩基毎に1分子のDIGが取り込まれます。
RNA標識反応の概要
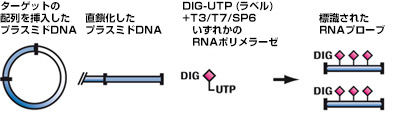
転写するDNAテンプレートをT7、SP6、またはT3 RNAポリメラーゼに対するプロモーターを持っている適切な転写ベクターのポリリンカー部位にクローニングします。適切な部位でテンプレートDNAを直鎖化した後、DIG-11-UTP存在下でRNAが転写されます。標準的な条件下では、1µgのテンプレートDNAから約10µgの完全長DIG標識RNAが転写されます。
RNAプローブ標識のヒント
DIGによってRNAプローブを標識する際に注意すべき箇所について、「RNase」「テンプレートの純度」「テンプレート配列」「テンプレート長」「プローブの保存」という5項目に分けてまとめました。以下に見ていきましょう。
まずはRNaseです。RNaseは遍在性が高く、活性に補因子を必要としません。実験を成功させるには、以下の手段によってRNaseによるコンタミネーションを回避する必要があります。
- ディスポーザブルのプラスチック容器や、RNase ZAPなどで消毒済みのガラス容器を使用する。
- あらゆる溶液にピロ炭酸ジエチル(DEPC)または二炭酸ジメチル(DMDC)処理をする。可能であればオートクレーブ処理をする。
- 実験中を通じ、実験用手袋を着用する。
次にテンプレートの純度です。ラベリング効率の大部分はテンプレート純度に影響されます。DNAテンプレートの純度を高く保ちましょう。ラベリング効率の大部分はテンプレート純度に影響されます。テンプレートは直鎖化し、フェノール/クロロフォルムで抽出し、エタノールで沈殿させましょう。
さらに、テンプレート配列ついて。特定のリボソームRNA(28sや18s)からの意図しないシグナルを弱めるため、テンプレートからは可能な限りポリリンカー配列を取り除いてください。また、不必要な配列が転写されることを避けるため、5'粘着末端あるいは平滑末端を生じる制限酵素を使用しましょう。
そして、テンプレート長。適正なテンプレート長は約1kb、最短のテンプレート長は200bpです。
最後に、プローブの保存です。RNAプローブを長期保存する場合には、分注して-20°Cまたは-70°Cで冷凍します。エタノール中のDIG-標識プローブは、-20°Cまたは-70°Cで約1年間安定しています。
以上、DIGシステムによってRNAを標識する方法と、使用時のヒントについて紹介しました。検出効率が悪い、コンタミするなど結果がうまく得られないときには、上記の注意点をひとつひとつ確認してみましょう。

下記フォームでは、M-hub(エムハブ)に対してのご意見、今後読んでみたい記事等のご要望を受け付けています。
メルクの各種キャンペーン、製品サポート、ご注文等に関するお問い合わせは下記リンク先にてお願いします。
*入力必須




