バッファー調製時のチェック項目(バッファーの基礎知識)

使用前に確認しておきたいバッファーの特徴
研究を成功させるためには実験条件に合ったバッファーを選ぶことが重要です。ライフサイエンス実験用として知られているバッファーでも、使用する試薬・サンプル・実験方法によっては使用に適さない場合があります。下のリストに使用前に確認しておきたいバッファーの特徴を6つにまとめてみましたので、ぜひチェックして、最適なバッファーを選ぶ参考にしてください!
■吸光スペクトル特性
240~700 nm(紫外線および可視光近傍)に吸収極大を持つ化合物は、通常のライフサイエンス実験のバッファーには使用できません。
■バッファーに用いる化合物のpKa
緩衝能を最大限に発揮させるために、実験条件のpHになるべく近いpKaをもつ化合物をバッファーとして選択しましょう。
■実験中のpH変化
実験中に起こるpH変化の傾向があらかじめ分かっている場合は、pH変化に拮抗するpKaをもつ化合物を選択しましょう。たとえば、実験中にpHが低下する時は、実験条件のpHよりもわずかに高いpKaの化合物が適しています。また逆に、pHが上昇する時は、実験条件のpHよりもわずかに低いpKaの化合物が適しています。
■特定の実験条件との相性
一部の弱酸や弱塩基には、バッファーとして使用できない実験条件があります。たとえば、クエン酸バッファーやリン酸バッファーは、カルシウムイオンに依存する実験系には使用できません。これは、クエン酸にはカルシウムイオンをキレートする性質があり、リン酸はカルシウムイオンと反応して不溶性のリン酸カルシウムを生じるからです。
■無機陽イオンの影響
酵素に対するイオン強度の効果測定を行うときは金属イオンを含まないバッファーを選択する必要があります。金属イオンを含まないバッファーの代表は、水酸化テトラメチルアンモニウム(Tetramethylammonium hydroxide: TMAH)バッファーです。生物に対して強い毒性を示すこの4 級アミンから調製された緩衝液は、任意の無機陽イオンを添加できるため、金属イオン要求性の酵素反応の評価実験等に利用されます。
■極性有機化合物とpH
生物学実験では、エタノールやメタノール等の水溶性の高い有機化合物を溶媒として使用する場合があります。これらの有機化合物は、非常に小さい解離定数をもつため、水溶液中に少量の添加する場合はpHに影響を与えません。逆に、メタノールやDMSOのような有機化合物の中にごくわずかな水が加わると、水分子からプロトンが解離し、系のpHが大きく下がるので注意しましょう。
次にバッファー調製のポイントを紹介します。
バッファー調製のポイント
■液温を考えたpH調整
記事「pHと酸解離定数pKaの関係」で紹介したとおり、水溶液の温度が上昇すると、緩衝作用をもつ化合物のpKaがわずかに下がります。pKaが下がるとpHも低下します。したがって、バッファー試薬の理論的な濃度や混合比率だけでなく、実験に使うときの液温を考えてpHを調整する必要があります。
■pH 調整
緩衝作用をもつ化合物を水に溶かしただけでは緩衝液にはなりません。溶液のpHをその化合物のpKaに近づけて初めて、緩衝効果が発揮されます。水に溶けた酸に対してpH調整を行う場合は水酸化ナトリウム、水酸化カリウム、アンモニアなどの塩基を加えます。塩基に対して調整するときは、塩酸などの酸を利用して、pHをpKaに近づけます。
■バッファー濃度
バッファーは使用時に調製するのがもっとも理想的です。あらかじめ作っておいて保管することはあまり推奨できませんが、ストック溶液を作って保存しておく場合も、最終的な希釈は、実験温度に近い温度で行うようにしましょう。
■リン酸ナトリウムバッファーの調製
リン酸は価数の異なるイオン形態をもち、二段階で電離します。この性質を利用して、リン酸ナトリウムバッファーを調製するときは、同濃度(0.1~0.2M)のリン酸ニ水素ナトリウム溶液とリン酸水素ニナトリウム溶液を以下の表に示す規定量比で混合します。
この手法は、二段階電離をする他の化合物(たとえば炭酸ナトリウムと重炭酸ナトリウム)にも応用できます。
■酸(または塩基)とその塩の活用
バッファーを調製する最も簡単な方法は、酸または塩基とその塩(塩基または酸)を混合することです。この方法は特に、同じ組成の異なるpH を持つ一連のバッファーを調製する際に効力を発揮します。たとえば、0.1 M HEPES(CAS: 7365-45-9、25 ℃におけるpKa = 7.48)と0.1 M HEPES・Na(CAS:75277-39-3、25℃におけるpKa = 7.55)を、1:10から10:1 の比率で混合すると、おおよそ6.55~8.55 の範囲のpHをもつ0.1 M HEPES バッファーを調製することができます。
■理論的な混合比率の算出
記事pHと酸解離定数pKaの関係で紹介したように、pHとpKaの関係は、pHの定義から①のように導かれ、pH – pKaをΔpH と書けば、この式の関係は下に示すようなグラフで表現できます。
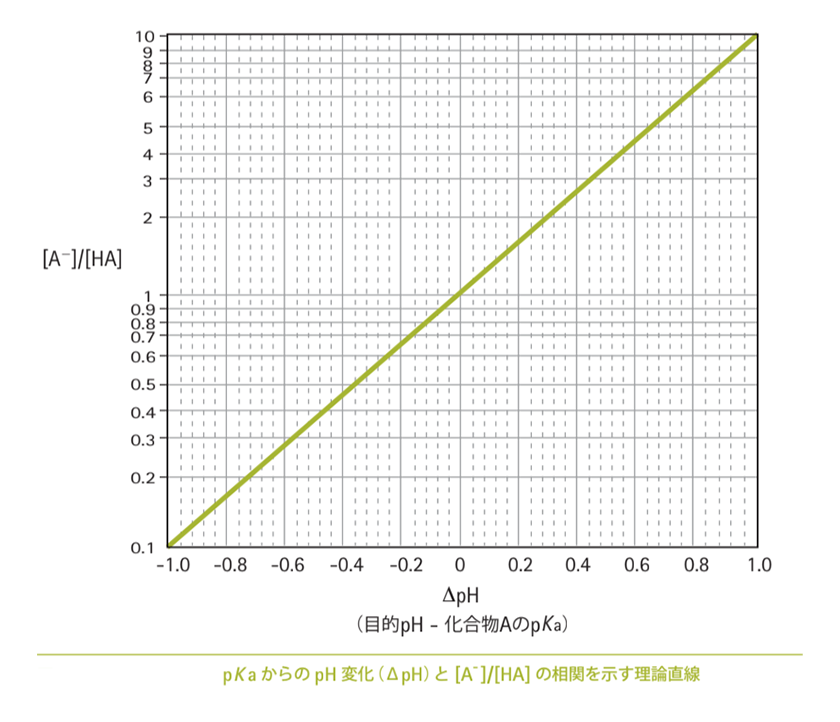
横軸ΔpHは、調整したいpHと使用する化合物のpKaの差なので、すぐに計算できます。ΔpHがわかれば、対応する縦軸の値から、酸と塩基の理論的な混合比率を算出できます。
たとえば20℃でpH 7.6 のMOPS(pKa 7.2)バッファーを調製する場合、横軸のΔpH は 0.4になります。このとき、グラフから縦軸の値を読み取ると2.5になるので、MOPSバッファーを調製するには、同濃度のMOPS・Na とMOPS を約2.5:1 の比率で混合すればいいことがわかります。
以上、バッファーの調製時と使用時のチェック項目を紹介しました。バッファーを使用する前には、これらの項目をしっかりと確認をしながら実験を進めていきましょう。

下記フォームでは、M-hub(エムハブ)に対してのご意見、今後読んでみたい記事等のご要望を受け付けています。
メルクの各種キャンペーン、製品サポート、ご注文等に関するお問い合わせは下記リンク先にてお願いします。
*入力必須




