<研究最前線>サイの目のブレイクスルー

「存在」でなく「機能」
―小松先生は「エンザイモミクス」という概念を提唱されていますが、これはどのようなものでしょうか。
生体内の分子を網羅的に調べる手法を「オミクス」と呼びます。エンザイモミクスは、酵素の作用を網羅的に解析しようというものです。酵素は知られているだけで5,000種類以上あります。これらには、どういう反応を触媒するかはわかっていても、どういうタイミングではたらくか、どういう病態に関わるかなどは未解明のものが多くあります。これを解析してゆこうというものです。
解析の手法として、我々は「酵素を光らせる」、つまり酵素のはたらきを蛍光分子で可視化する方法を主に用いています。たとえばガラクトシダーゼを検出するには、ガラクトースと蛍光化合物が結合した形の化合物(蛍光プローブ)を用います。ガラクトシダーゼがはたらくと糖部分が切断され、蛍光化合物が発生するため、酵素の存在がわかります。
―タンパク質の網羅的解析を行なう「プロテオミクス」とは、また違った概念なのですね。
タンパク質がそこに存在しているということと、酵素として活性を示しているということは、必ずしもイコールではありません。酵素の存在ではなく、機能そのものを網羅的に解析しようということです。その解析ツールは、たとえば医薬の標的になる酵素を見つけ出すとか、がんの診断につながるなど、非常に優れた武器になりえます。
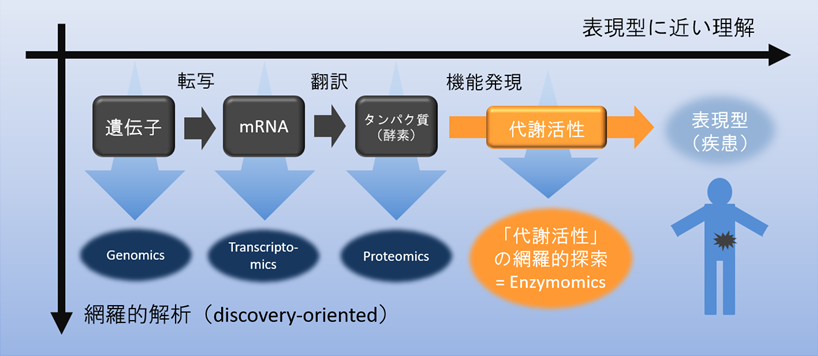
図.“Enzymomics”の概念(小松先生作成)
―どのような解析方法ですか?
我々がエンザイモミクスという言葉を使う前から、相当する研究を行なっている人はいました。私の留学先の先生であるBenjamin F. Cravatt教授もその一人で、大きく影響を受けています。帰国してから、彼らの後追いでは仕方ないと、自分たちの強みを活かした方法を考えました。要するに、解析したいサンプルに多数の蛍光プローブを加え、どの酵素がはたらいているかを、蛍光によって可視化するというものです。たとえば、正常時のサンプルと疾患時のサンプルを解析して比較することで、疾患に関与する酵素を見つけ出せる可能性があります。
そこでまず、サンプルを二次元電気泳動で展開し、蛍光プローブを加えて酵素活性を検出する方法を試みました。蛍光プローブは、各種ペプチドなどの置換基が蛍光化合物と結合させてあり、酵素によって切断されると光る仕組みです。ただこの方法では、生じた蛍光化合物がゲル内で拡散してしまい、スポットを決定できないことが問題になりました。
―どう解決されたのでしょうか?
ハンドブックに載っている方法などいろいろ試したのですがうまく行かなかったので、電気泳動を行なった後、ゲルを細かく裁断してしまう方法を考えました。これですと拡散が起こらず、どこに酵素が存在するかを正確に決められます。いわばトコロテン方式ですね。裁断の仕方も試行錯誤したのですが、結局ホームセンターで買うことのできる、目の細かい網戸を使って切る方法がうまく行きました。
―アミドを切る酵素を、網戸で切って見つけたというシャレのような話ですね(笑)。
プラスチック成形の技術を持った方に、効率的に切断する道具を開発していただきました。その後、SAINOMEというベンチャー企業を起こされています。こうした方と知り合えるのも縁ですね。この方法の確立により、0.1ng程度の酵素をその活性に応じて検出するという技術が実現しました。

広がるエンザイモミクスの世界
―この方法の成果は?
肺炎マウスの肺胞洗浄液の網羅的解析により、ペプチドN末端のN-ホルミルメチオニンを切断する酵素の活性が上昇していることを見出しました。分析の結果、アシルアミノ酸切断酵素(APEH)が関与していることがわかりました。質量分析を行なうと、いくつか候補のタンパク質を表示してくれるのですが、そこでこうした「当たり」らしき酵素が入っていると「やった!」という気になります。
その他、大腸がんの細胞でニューロライシンという酵素の活性が上昇しているなど、疾患に関連した酵素をいくつか見つけ出しています。この酵素がどのように病態と関わっているのか、また診断に利用可能か、現在検証を進めています。
また、見つけた酵素の阻害剤をスクリーニングで見つけ出し、機能を検証するようなことも、進めています。低コストで化合物ライブラリが利用できる環境ですので、その点は非常にありがたいです。
―今後の展開をどう考えておられますか?
小松 酵素検出の網羅性を上げる必要があると思っています。今のところ、プロテアーゼやグリコシダーゼといった、結合を切断する酵素は容易に蛍光プローブで検出できます。しかし、たとえばプロリルイソメラーゼ(プロリン残基のアミド結合のシス・トランス異性化を触媒する酵素)のようなケースは、酵素活性を検出するプローブは作られていません。こうした構造変化をどう蛍光強度の変化に落とし込むか、検討を進めています。質量分析ではどうしようもない酵素ですので、蛍光プローブで検出できれば大きな価値があると思います。
―まだまだ研究すべきことが多く、楽しみですね。
<プロフィール>
小松徹(こまつとおる)
東京大学大学院薬学系研究科 薬品代謝化学教室 特任助教
1981年生。2009年 東京大学 大学院薬学系研究科 博士課程 修了(長野哲雄教授)。2008-2009年 日本学術振興会 特別研究員(DC2)。2009-2010年 日本学術振興会 特別研究員(PD)(井上尊生助教授/米国 Johns Hopkins大学)。2010年 日本学術振興会海外特別研究員(Benjamin Cravatt教授/米国 Scripps研究所)、2010年から現職。2013-2016年 独立行政法人 科学技術振興機構(JST)さきがけ 個人研究者兼務。
<論文Pick Up!>
- Discovery of cell-type-specific and disease-related enzymatic activity changes via global evaluation of peptide metabolism. Onagi, J.; Komatsu, T.; Ichihashi, Y.; Kuriki, Y.; Kamiya, M.; Terai, T.; Ueno, T.; Hanaoka, K.; Matsuzaki, H.; Hata, K.; Watanabe, T.; Nagano, T.; Urano, Y. J. Am. Chem. Soc., 2017, 139, 3465–3472.
- Development of chemical tools to monitor and control isoaspartyl peptide methyltransferase activity. Kimura, Y.; Komatsu, T.; Yanagi, K.; Hanaoka, K.; Ueno, T.; Terai, T.; Kojima, H.; Okabe, T.; Nagano, T.; Urano, Y. Angew. Chem. Int. Ed., 2017, 56, 153–157.

下記フォームでは、M-hub(エムハブ)に対してのご意見、今後読んでみたい記事等のご要望を受け付けています。
メルクの各種キャンペーン、製品サポート、ご注文等に関するお問い合わせは下記リンク先にてお願いします。
*入力必須