<研究最前線>三浦正幸-細胞死を軸に広い視野で発生や成長をとらえる

東京大学大学院薬学系研究科教授の三浦正幸先生は、細胞死の研究を主軸としながら、発生や成長におけるサイズ制御や、再生における代謝制御、栄養と腸内細菌の関係など、多様な研究を行っています。三浦先生の遺伝学教室で取り組んでいる主な研究テーマについて、お話を伺いました。
細胞増殖と細胞死の協調
-現在の研究テーマを教えてください。
私たちの研究テーマは、大きく言うと発生生物学という分野です。受精してから生物としての体ができあがるまで、最初は無個性だった細胞の性質が変化して様々な組織を形成します。そのとき、細胞が増殖すると同時に多くの細胞が死んでいるのです。このような細胞死に特に興味を持っています。
例えばニワトリの足が作られるとき、最初は水かきがあるのですが、発生が進むにつれて足の指の間の細胞だけが自発的に死んで取り除かれてなくなります。このような細胞死はプログラム細胞死とよばれています。「作りながら壊す」という、一見すると無駄に思える現象が、生物の発生ではよくあることなのです。ここから発生、成長、さらには老化や再生など、様々な研究テーマが派生しています。
-三浦先生が細胞死の研究を始めたきっかけは何ですか?
どうやって細胞の運命が決まるのかということに興味があって、研究の世界に入りました。線虫の発生においてプログラム細胞死を引き起こす遺伝子ced-3を同定した一人であるJunying Yuan先生の研究室に留学する機会があり、私はマウスの発生を研究していたので、哺乳類で細胞死に関わる因子を探索することになりました。そこで細胞死を引き起こすタンパク質分解酵素「カスパーゼ」が哺乳類にもあることを世界に先駆けて示すことができ、そこから今の細胞死の研究に至っています。現在の研究材料は、主にショウジョウバエを用いています。
-具体的にはどのような研究を行っているのですか?
カスパーゼが活性化することで生じるプログラム細胞死である「アポトーシス」を研究しています。作りながら壊している状況について、ショウジョウバエの幼虫がサナギになってから羽化する間に何が起きているのか、ライブイメージングによって解析しています。サナギでは表皮の細胞が幼虫のものから成虫のものに入れ替わるのですが、このとき幼虫上皮で一斉に細胞死が起きるのではなく、徐々にカスパーゼが活性化して細胞死が起きるのです。細胞死に接したところから成虫細胞(組織芽細胞)の増殖が伝播します。その様子をライブイメージングでとらえることができます。この段階でカスパーゼの活性を阻害すると組織芽細胞が増殖せず、逆に組織芽細胞の増殖を抑制すると今度はアポトーシスが起きません。細胞の増殖と死がコーディネーション(協調)しているのです。より正確に述べると、アポトーシスが起きると同時に細胞増殖や再生を促すシグナル分子が分泌されるのです。これは、培養細胞ではわからない、生体でないと観察できない現象です。
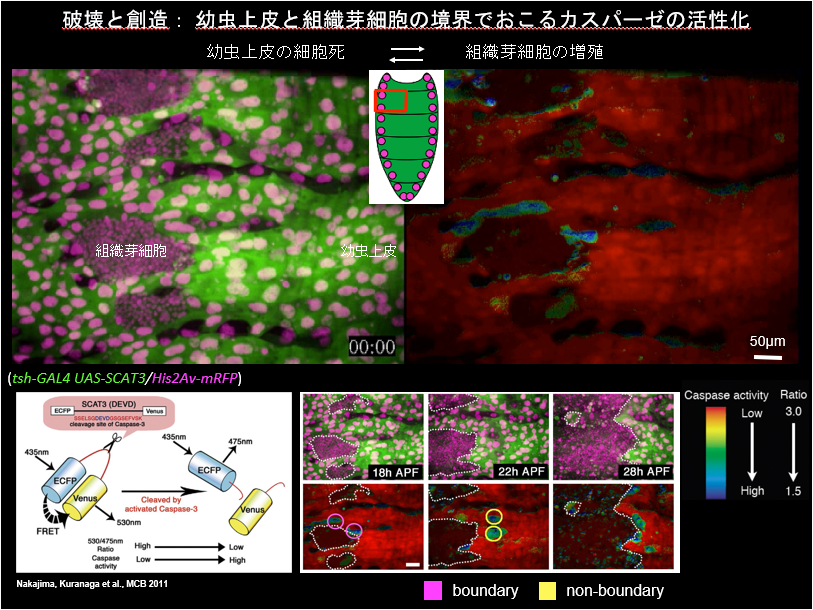
幼虫上皮と組織芽細胞の接するところでカスパーゼ活性が高い(青いところ)
-カスパーゼは何のシグナルを受けて活性化するのですか?
あまりはっきりとわかっていないのですが、圧力が可能性の一つとして挙げられています。例えば、サナギの中で成虫の背中が作られるとき、成虫原基が左右から移動して融合するのですが、融合するとき背中の真ん中だけカスパーゼが活性化して細胞が脱落します。融合の際、細胞密度が上昇して圧力がかかるため、混雑による細胞死が起きているのではないかという考えが、この分野で話題になっています。
細胞死とは異なるカスパーゼの機能
-他にはどのような研究テーマを持っていますか?
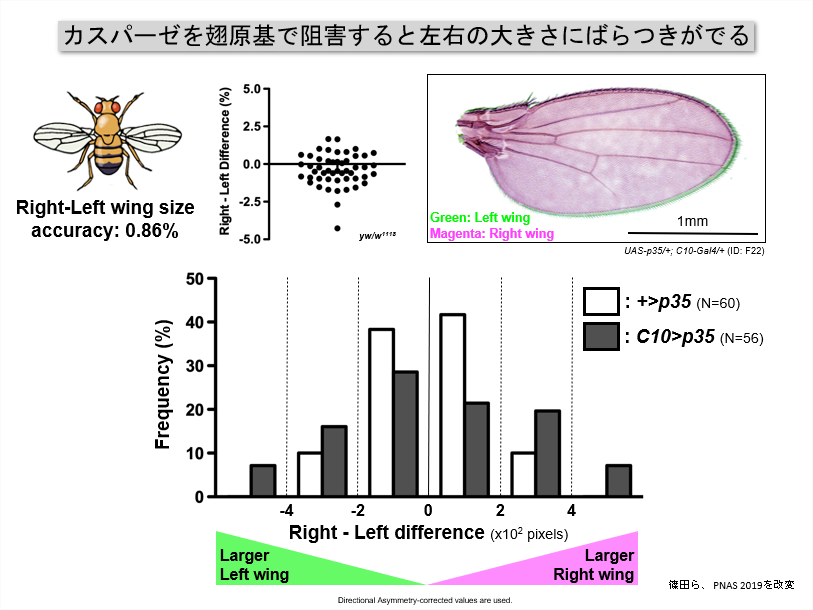
カスパーゼには様々な種類(カスパーゼファミリータンパク質)があり、アポトーシスを引き起こすだけでなく、正しい発生を誘導していることが最近わかってきました。例えば、翅原基でカスパーゼの活性化を阻害したとします。アポトーシスが抑制されるので、生き残る細胞の数が増えて成虫の翅のサイズが大きくなるだろうと予想できますよね。ところが逆に小さくなってしまうのです。
それだけでなく、翅の面積が左右で異なる、つまり左右相称性が乱れることもわかりました。これは私たちの教室の篠田夏樹さんの発見です(https://www.pnas.org/content/116/41/20539)。
翅の大きさ以外にも、ショウジョウバエの背中には触覚の外感覚器として左右に2本ずつ毛が生えているのですが、カスパーゼの活性化を抑制すると片方だけ3本になってしまう現象も観察されました(https://doi.org/10.1038/sj.emboj.7600822)。
-アポトーシスが左右相称性に関与するということですか?
ショウジョウバエの場合、カスパーゼファミリーの中でもDcp-1とDecayとよばれているものは、確かに翅の形成に関与するのです。しかし、これらの発現を抑制しても翅の成虫原基でアポトーシスに変化はなかったのです。つまりDcp-1とDecayはアポトーシスを誘導せずに、翅の形成に関与し、大きさなどの左右相称性といった表現形を安定化させるのに寄与することを明らかにしました。
-では、カスパーゼは何を分解するのですか?
このときの研究では、細胞内の分解機構の1つであるオートファジーを促進するAcinusというタンパク質をDcp-1が分解して翅の成長に関与することがわかったのですが、他のタンパク質も標的にしているのかもしれません。それはこれからの課題で、現在非常に強い興味を持って研究をしているところです。
-カスパーゼがアポトーシス以外にも関与していることは初耳でした。
これまでアポトーシスは培養細胞を使ったシグナルの研究が多く、生体を使った発生の安定性に注目する人はあまりいませんでした。その分、これから研究がどう発展するかというのは面白いかなと思っています。
再生時のメタボローム解析、栄養と腸内細菌
-発生以外のテーマでも研究をされているとお聞きしました。
再生の研究も行っています。ショウジョウバエの翅の成虫原基は再生能が高く、遺伝子改変によって一時的に毒素を発現させて損傷しても、発現をやめるとちゃんと再生します。私たちはこのとき、損傷領域周辺の環境が重要ではないかと考え、体液のメタボローム解析を行いました。採取できる体液量が少ないので大変だったのですが(笑)。その結果、再生中にメチオニン代謝が変化することがわかりました。さらに、脂肪体でメチオニン代謝関連遺伝子の発現を局所的に抑制すると翅が再生しないことも判明しました(https://www.pnas.org/content/113/7/1835)。つまり、脂肪体におけるメチオニン代謝が翅の再生に関与しているのです。これは教室の樫尾宗志朗さんの発見によるものです。
-翅の成虫原基と脂肪体とは距離が離れていますが、どのようにシグナルが伝達するのですか?
どの因子が応答に関与しているか、というところまではまだ突き止めることができていません。他にも、表皮が損傷するとなぜか腸の細胞の応答も見られます。現在は、どうやって再生シグナルが惹起され、どう遠隔組織から伝達されて再生が起こるのか、というところにフォーカスしています。これもやはり培養細胞では見ることのできない、生体でなければ観察できない現象ですね。
-他にも、栄養と腸内細菌についても研究をされておられますね。
これは講師の小幡史明さんがやられているテーマです。最近ヒトにおいて、胎児や幼少期における飢餓や環境ストレスが大人になってからの糖尿病などの発症リスクに関係することが疫学研究から報告されています。これについてはDOHaD(Developmental Origins of Health and Disease)という仮説が提唱されていますが、この説の検証にショウジョウバエがよいモデルになると考えています。
彼が見つけたのがすごく面白い現象で、ショウジョウバエの幼虫に低量の酸化剤を食べさせると、幼虫期だけでなく成虫になっても腸内細菌叢の組成変化が継続し、寿命が延長することを発見しました(https://www.nature.com/articles/s41467-018-03070-w)。その理由については現在研究中です。ヒトでは疫学的な解析が中心ですが、ショウジョウバエであれば遺伝子改変に加えて餌のアミノ酸などの栄養素や細菌叢を変えるなど、多くの工夫ができます。こうすることでDOHaDの仕組みに迫ることができるのでは、と考えています。
見たときに感じた疑問をそのまま研究する
-薬学部に所属されておられるので、今の研究をヒトに応用することを将来的には考えていらっしゃるのですか?
同じような質問を私たちの教室に見学に来る学生からほぼ必ず聞かれるのですが、ヒトへの応用は考えていません。大学院生のときにマウスの発生をやっていたので、疾患との関係に興味はあります。ただ、具体的にこの疾患を治したいという興味ではなくて、正常が異常になったときになぜ疾患になるのか、というところに興味があります。
-そもそも正常な状態で何が起きているのか、どこかが異常になったときにどのような変化が起きるのか、というところにまず焦点を当てているのですね。
そうです。でも他の専門分野の研究者たちと話をすると、私の研究に興味を持っていただけることはよくあります。いろいろなグラントの班会議などで医師の方々とお話しするのも楽しいですよ。カスパーゼによるアポトーシスが細胞増殖を誘導する現象などは、応用範囲が広いと思います。
-研究テーマが多岐にわたっていて他の分野にも興味があると思いますが、実際に先生の教室で取り組むかどうかの線引きはどのように決めておられますか?
勘、ですかね(笑)。面白いと思うか思わないか。あとは、この教室にある実験材料やノウハウなどの財産、つまり強みを最大限活用できるか、ですね。作戦としては、そういうことがあります。
-使い慣れた材料だからこそ、違うテーマで実験しても新しいものが見えてくる、と。
そうです。みんな「カスパーゼと言えば細胞死」と考えていたところに、組織のサイズ制御という視点で実験したら予想と違う結果が得られて、「これは変だな」というところから研究が始まったわけですから。見たときに感じた疑問をそのまま研究するというスタイルで私たちはやっています。そのときに、実験する材料は揃っているので、他の人よりも早く面白い仕組みにたどり着けるかな、という期待を持っています。
-視野が広いのですね。
散漫なだけです(笑)。疑問を見つけたら研究テーマは広がってしまうものですから。
<プロフィール>
三浦正幸(みうらまさゆき)
東京大学大学院薬学系研究科 遺伝学教室 教授
1960年生。1988年 大阪大学 理学研究科 博士課程 修了(御子柴克彦教授)。1988-1989年 日本学術振興会 特別研究員(御子柴克彦教授/基礎生物学研究所)。1989-1994年 慶應義塾大学医学部助手(植村慶一教授)。1992-1994年 NIH Fogarty International Research Fellow (Junying Yuan准教授/米国マサチューセッツ総合病院)。1995-1997年 筑波大学基礎医学系講師(岡野栄之教授)。1997-2001年 大阪大学医学部助教授(岡野栄之教授)。2001-2003年 理化学研究所脳科学総合研究センターチームリーダー。2003年から現職。

下記フォームでは、M-hub(エムハブ)に対してのご意見、今後読んでみたい記事等のご要望を受け付けています。
メルクの各種キャンペーン、製品サポート、ご注文等に関するお問い合わせは下記リンク先にてお願いします。
*入力必須




