TrueGel3Dによる3D培養 その概要と使用例
期待が高まる3D培養技術
従来の二次元的な細胞培養(2D)は、細胞が平面に増殖するため、生体内の立体的な環境とは異なる状態であるという課題がありました。一方、3D培養(3次元培養)は、細胞が立体的に増殖可能で、生体内により近い構造で研究することができます。
したがって、オルガノイド作成など従来の平面的な培養では行えなかった組織の形成や、再生医療への応用、生体内に近い立体的な環境下での薬物動態の分析、細胞間相互作用の研究など、3D培養ならではの研究成果が期待されています。
3D培養を行う際の「足場」には、様々な支持体が選択肢となりますが、その一つが、Sigma-AldrichのTrueGel3Dです。この記事では、TrueGel3Dを用いた3D培養の概要と、実際の使用例について紹介します。
TrueGel3Dとその特長
TrueGel3Dは、様々な種類の細胞で実績のある3D培養用のハイドロゲルで、ポリマーとクロスリンカーを混合するとゲルが形成されます。複数のキットが販売されており、用途に合わせて選択することができます。TrueGel3Dは動物由来成分を含まないため、実験結果の分析を妨げたり、細胞を汚染したりする可能性がありません。さらに、一部のTrueGelに含まれるRGDペプチドは、生体の細胞外マトリックス(ECM)の重要な機能を模倣することができます。また、透明で観察しやすいという特長もあります。
以上の理由から、TrueGel3Dテクノロジーは、3D環境での細胞の形態学的および生理学的特性を調べるためのツールとして有用といえます。
3D培養を構成する4つのコンポーネント
TrueGel3Dによる3D培養は次の4つのコンポーネントで構成されています。
-
TrueGel3Dポリマー:ポリビニルアルコール(以下、PVA)またはデキストランから選択します。
-
クロスリンカー:両端にあるチオール基でポリマー上のチオール反応基と結合します。これによってポリマー鎖を連結し、ゲルを形成します。ポリエチレングリコール(以下、PEG)または細胞分解性(cell-degradable:以下、CD)クロスリンカーの2種類から選択可能です。
-
接着因子:マトリックスへの細胞接着や細胞の移動が必要な場合、TrueGel3D Arg-Gly-Asp(以下、RGD)インテグリン接着ペプチドのような接着配列を含むペプチドをゲルに加えることができます。ほかにも、細胞外マトリックスタンパク質(例:フィブロネクチン、ラミニン)、ペプチド、ヘパラン硫酸または成長因子(キットには含まれません)など他の生理活性物質の添加も可能です。
-
細胞(細胞はキットに含まれません)

TrueGel3Dキットの使い方とプロトコール
TrueGel3Dは、キットの試薬と細胞を混ぜるだけで3D培養を開始することができます。以下はゆっくり固まるタイプのTrueGel3Dキット(製品番号TRUE6-1KTなど)を使用する場合の手順です。
-
ポリマーをミックスする:PVAまたはデキストランでベースが作られます。
-
ペプチドをミックスする:マトリックスへの細胞接着や細胞の移動が必要な場合はRGDペプチドを添加します。
-
細胞をミックスする:用意した細胞を加えます。(細胞はキットに含まれません)
-
クロスリンカーを加え、ゲル化させる:細胞が分解できないクロスリンカー(PEG)と細胞が分解できるクロスリンカー(CD)があります
-
培養する:プレートに移して液体培地でインキュベートします

速く固まるタイプのTrueGel3Dキットの場合は、クロスリンカーをあらかじめプレートに分注し、そこに細胞とポリマー、ペプチド(ペプチドはオプション)のミックスを添加すると、そのままプレート上でゲルが形成されます。
なお、TRUE1-1KT以外のキットにはRGDペプチドは含まれていないので注意しましょう(別売)。
TrueGel3Dの使用例
TrueGel3DはMDCK細胞、線維芽細胞、癌細胞、初代細胞、間質細胞および胚性心筋細胞など多くの細胞種で実績があります。
-
MDCK細胞のシスト形成
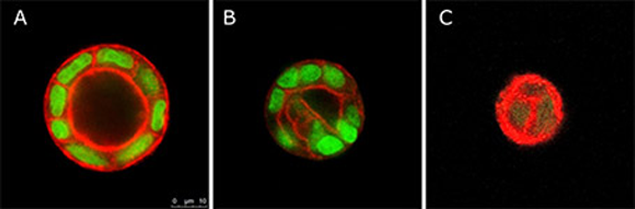
TrueGel3D FAST-PVAハイドロゲルにRGD integrin adhesion peptideを加えMDCK細胞を15日間培養した結果、細胞単層の内腔が観察されました(図1-A)。TrueGel3D FAST-PVAハイドロゲルにscrambled RGD peptideを添加した場合、MDCKシストは内腔が見られましたが、偏極した細胞は見られませんでした(図1-B)。TrueGel3D FAST-PVAハイドロゲルにthioglycerolを添加して増殖したMDCKは、管腔も偏極した細胞も見られませんでした(図1-C)。

<資料より>
図1:MDCK細胞をTrueGel3D FAST-PVAハイドロゲルで15日間培養後、形成された嚢胞の融合共焦点画像(緑:核、赤:アクチン細胞骨格)
手順やデータの詳細は資料「Cyst Formation of MDCK Cells in TrueGel3D™ Hydrogels」をご覧ください。
-
3T3線維芽細胞
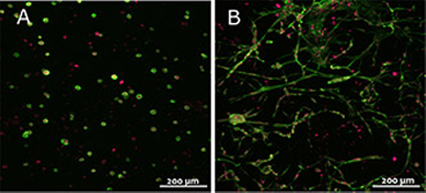
PEG非細胞分解性クロスリンカーを含むTrueGel3Dハイドロゲルで増殖した3T3線維芽細胞は、丸く、緻密に凝集した凝集体を生じ(図2-A)、CD-細胞分解性クロスリンカーを含むTrueGel3Dハイドロゲルで増殖した細胞は、広がって増殖しました(図2-B)。A、BともにRGD integrin adhesion peptideを加えています。

<資料より>
図2:TrueGel3D FAST-PVAハイドロゲル中の3T3線維芽細胞。TrueGel3D RGD integrin adhesion peptideを加え、PEG非細胞分解性クロスリンカー(A)またはCD-細胞分解性クロスリンカー(B)で架橋した。(緑:核、赤:アクチン細胞骨格)
手順やデータの詳細は、資料「Utilization of TrueGel3D™ Hydrogels to Study Fibroblast Spreading」をご覧ください。
-
腫瘍細胞と間質細胞の共培養
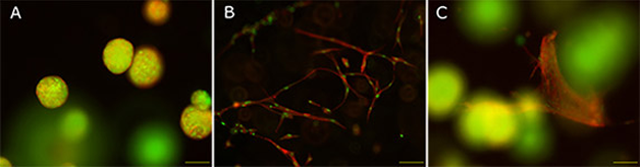
TrueGel3Dハイドロゲル中で、MCF-7乳癌細胞株を単独で培養した場合は腫瘍様のスフェロイドを形成し(図3-A)、ヒト真皮線維芽細胞を単独で培養した場合は伸びた状態が見られました(図3-B)。TrueGel3Dハイドロゲルで両方の細胞を共培養した場合、14日後も生理学的および形態学的特徴を保持し、腫瘍微小環境を研究するための腫瘍-間質モデルとなる状態が観察されました(図3-C)。A、B、CのいずれもRGD integrin adhesion peptideを加えています。

<資料より>
図3:TrueGel3D™ハイドロゲル中におけるMCF-7乳癌細胞株とヒト真皮線維芽細胞の単独および共培養(緑:核、赤:アクチン細胞骨格)
手順やデータの詳細は、資料「Co-culture of Tumor and Stromal Cells in TrueGel3D™ Hydrogels」をご覧ください。
-
心筋の拍動の再現
ニワトリ胚の心組織から調製した細胞懸濁液を、デキストランポリマーとCDクロスリンカーで架橋し、RGDペプチドを含むハイドロゲルで培養しました(TRUE1)。 心筋細胞の凝集体が線維芽細胞に囲まれています。
※心筋細胞は、Dr. Udo Kraushaar(NMI Reutlingen(www.nmi.de/en/)、Electrophysiology Group、ドイツ)のご好意により提供されました。
TrueGel3Dハイドロゲルで培養した心筋細胞の拍動
以上、TrueGel3Dを用いた3D培養の概要と、実際の使用例について紹介しました。3D培養は、in vivo環境に近い状態で細胞を培養できるin vitro技術として、今後も活用が広がるでしょう。簡便なキットを用いて、より手軽に3D培養を取り入れてみてください。
<無料PDFダウンロード> 細胞培養ガイド
~ヒトやマウス・ラット細胞、ES/iPS細胞まで~
このガイドブックでは、細胞培養に必要な基本的知識、注意点、一般的なプロトコルおよび細胞培養に必要な培地、添加剤などをご紹介しています。
▼こんな方にオススメ
・これから細胞培養実験をはじめる方
・コンタミネーションせずに細胞培養したい方
・浮遊性細胞の継代方法や細胞の凍結/融解についてあまり自信がない方

下記フォームでは、M-hub(エムハブ)に対してのご意見、今後読んでみたい記事等のご要望を受け付けています。
メルクの各種キャンペーン、製品サポート、ご注文等に関するお問い合わせは下記リンク先にてお願いします。
*入力必須