食品分析の強い味方!QuEChERS法のすすめ

食の安全に貢献、QuEChERS(キャッチャーズ)法
食品中に残留する農薬や飼料添加物、動物用医薬品について、「一定の量を超えて農薬等が残留する食品の販売を禁止する」という新しい制度が2006年に施行されました。これにより、残留基準がある農薬等は約250種から約800種へと拡大。食の安心と安全への関心が高まるなか、農薬を効率よく、迅速かつ正確に分析することが求められています。
残留農薬分析の前処理には、手間のかかる液液抽出や、煩雑な固相抽出法が用いられていました。しかし、近年になり海外の研究者がより迅速で簡易的な一斉分析法であるQuEChERS法を報告。国内においても広く普及するようになりました。 本記事では、このQuEChERS法の概要と操作手順について紹介します。
QuEChERS法の名前の由来
QuEChERS法は、塩類や精製用の充填剤をサンプルとともに撹拌・遠心分離する分散固相抽出(dSPE)による試料前処理法です。その名称はQuick(迅速)、Easy(簡単)、Cheap(安価)、Effective(効果的)、Rugged(堅牢性)、Safe(安全)の頭文字を合わせたもので、2003年に最初の報告が発表されました。
各項目の詳細は次の通りです。
- Quick(迅速):前処理時間は約10分。10サンプルを同時に処理した場合1時間未満で処理できます。
- Easy (簡単):複雑な操作は不要。
- Cheap (安価):高額な機器は不要。また使用する消耗品はいずれも安価。
- Effective (効果的):少量のサンプルで野菜から肉まで広範囲にわたり適用可能。また、妨害を減少させ実験誤差を最小限に抑える。
- Rugged (堅牢):何百ものサンプルをこなすルーチン分析に効率的な方法。
- Safe (安全):有害な化学物質や塩素系溶媒は不使用。また、1サンプルあたりの溶媒の使用量は約10~12mLと少量で、安全に貢献。
QuEChERS法は食品や農作物中の残留農薬分析に広く使われる他、近年では、PAH、PCB、PBDE、難燃剤などの分析へと発展しています3。
QuEChERS法の操作手順
QuEChERS法は、基本的に抽出と精製の2ステップで行います。アセトニトリルと塩類およびバッファーで分析対象物をマトリックスから抽出。精製時にPSA、C18、GCB(グラファイトカーボンブラック)、Z-Sepを使用することで、糖、脂質、ステロール、有機酸、タンパク質、カロチノイド、クロロフィルなどを除去します。
オリジナルのQuEChERS法は、弱酸性(pH 5-6)の条件下で水分含有量の多い(>80%)果物や野菜に有効であることが証明されています1-4。しかし、この条件に当てはまらない水分含有量の低い食品についても、表1に示すように抽出を行う前にサンプルへ水を添加することによって抽出効率を改善することができます。

表1 試料別水添加量
酸性の食品からの干渉を減少させるには5、pHの調整が必要です。例えばEN法では、クエン酸を使用し、抽出液をpH5-6に調整することで、酸または塩基に不安定な農薬を安定化させることができます3。
また、オリジナルの方法では低いpH(pH<3)である柑橘類には適応することができませんでした。しかし、ENの手法ではpHを調整することで、一般的な非酸性の食品と同様に高品質のデータを得ることができます。EN法の場合、5Nの水酸化ナトリウム溶液を塩混合物チューブへさらに添加し、レモンやライムなどには、5Nの水酸化ナトリウムを600μL3、ラズベリーのような作物には200μLを添加することが推奨されています。
クエン酸によりpH調整可能なEN法の具体的な手順について
QuEChERS法には主に2種類の方法があります。その中の一つ、EN法(EN15662:20081,2)は極性干渉の制限や、塩基センシティブな化合物を保護するため、NaClと複数のクエン酸ベースのバッファーを含んでいます。注意点として、クエン酸塩ステップでは水酸化ナトリウムの使用を避けてください。理由は精製のステップにおいて使われる充填剤にダメージを与えるからです。
EN法の具体的な手順は以下のとおりです。
- 試料の前処理
-20℃で凍結させた試料を流動性粉末となるまでドライアイスと共にホモジナイズします。 - 抽出
試料10gを50mLの遠沈管に測り取り、10mLのアセトニトリル+100uLの内部標準物質を加えて1分間攪拌します。次に、Supel™ QuE Citrate Extraction Tube(55227-U)の中身を加え、1分間撹拌した後、5分間遠心分離(3000rpm/min)を行います。 - 精製
アセトニトリル層(上澄み)を分取し、Supel QuE dSPE CLEAN-UP TUBEに添加します。およそ30秒撹拌(ENVI-Carb™を使用する場合は2分撹拌)した後、5分間遠心分離(3000rpm/min)を行います。上澄みを分取し、5%ギ酸/アセトニトリル溶液でpHを調整し、上澄み1mLに対し10μL添加します。
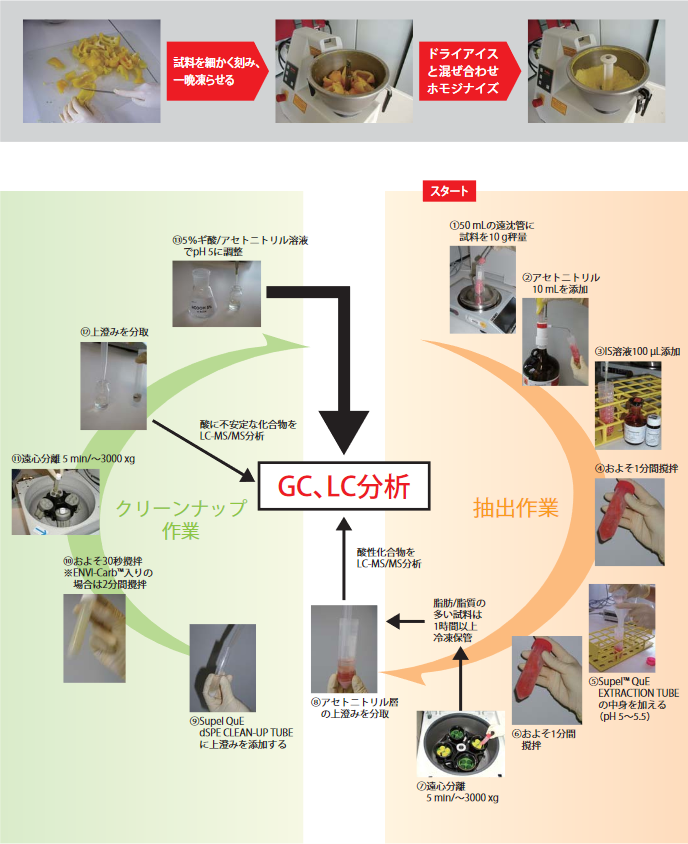
図1 EN法の前処理例
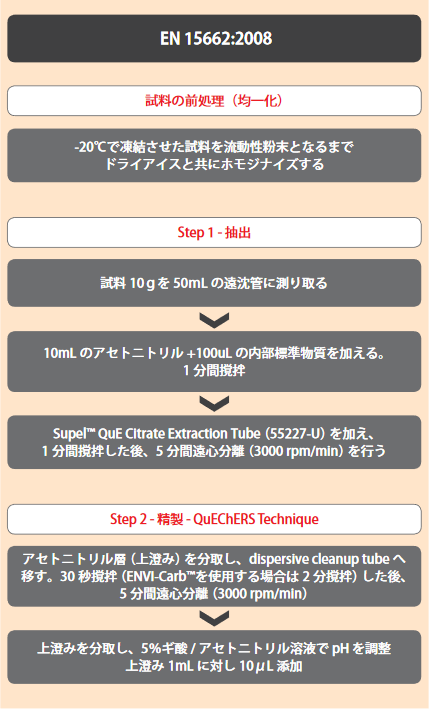
図2 EN法の流れ
pHに敏感な化合物の回収に優れたAOAC法
AOAC法(AOAC 2007.01.1)は、他のQuEChERS法と比べ、pHに敏感な化合物に対して優れた回収率を発揮するQuEChERS法です。
AOAC法の抽出では、塩に敏感な分析物を分解から保護するために、酢酸ナトリウムバッファーと1%酢酸のアセトニトリル溶液を使用します。以下で具体的な方法を解説します。
- 試料の前処理(均一化)
-20℃で凍結させた試料を流動性粉末となるまでドライアイスと共にホモジナイズします。 - 抽出
10-15gの均一化された試料を50mLのPTFE製遠沈管へ移します。15gの試料に対し、1%酢酸/アセトニトリル溶液を15mL+Supel QuE Acetate(AC)Tube(55234-U)+75μLの内部標準物質を加え、1分間撹拌し、その後1分間遠心分離(1500rpm/min)を行います。 - 精製
アセトニトリル層(上澄み)を分取し、dispersive cleanup tubeへ移します。30秒撹拌(ENVI-Carb™を使用する場合は2分撹拌)した後、1分間遠心分離(1500rpm/min)を行います。クロマトグラフィー分析の前に、ギ酸の追加やトルエンによる再構成など更なる処理が必要となる場合があります。
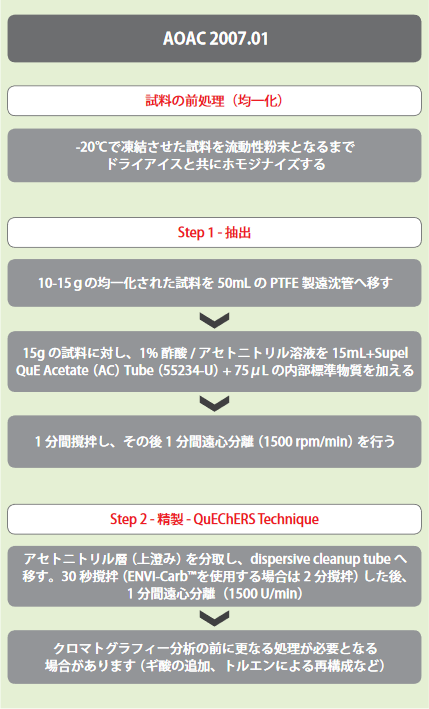
図3 AOAC法の流れ
このようにQuEChERS法は通常の固相抽出法よりも簡易で、作業効率を大幅に向上させられること、溶媒の使用量を少量でおさえることが可能であることがわかります。
メルクのサイトではカスタム製品の提供を行っています。「ラボでQuEChERS法の導入を考えている」、「QuEChERS法を採用しているが良好な結果が得られない」という人は、ぜひ一度利用してみてくださいね。
関連製品カタログのダウンロードはこちら
技術的なお問い合わせはこちら
参考文献:
1. Fast and Easy Multiresidue Method Employing Acetonitrile Extraction/Partitioning and “Dispersive Solid-Phase Extraction” for the Determination of Pesticide Residues in Produce. (M. Anastassiades, S.J. Lehotay, D. Stajnbaher,F.J. Schenck, J. AOAC International 86 (2003) 412).
2. Pesticide Residues in Foods by Acetonitrile Extraction and Partitioning with Magnesium Sulfate. (AOAC Official Method 2007.01).
3. Foods of Plant Origin̶Determination of Pesticide Residues Using GC-MSand/or LC-MS/MS Following Acetonitrile Extraction/Partitioning and Clean-upby Dispersive SPE (QuEChERS-method). (EN 15662 Version 2008).
4. Comparison of QuEChERS sample preparation methods for the analysis of pesticide residues in fruits and vegetables. (S. Lehotay, K. Son, H. Kwon, U. Koesukwiwat, W. Fu,K. Mastovska, E. Hoh, N. Leepipatpiboon, J. Chromatogr. A, 1217 (2010) 2548).
5. The QuEChERS Method ‒Background Information and Recent Developments, Community Reference Laboratory Pesticide Residues using Single Residue Methods. (M. Anastassiades, 1st Joint CRL-Workshop ‒Stuttgart, presentation (2006)).

下記フォームでは、M-hub(エムハブ)に対してのご意見、今後読んでみたい記事等のご要望を受け付けています。
メルクの各種キャンペーン、製品サポート、ご注文等に関するお問い合わせは下記リンク先にてお願いします。
*入力必須